自2002 年4月1日起 ,新加坡产品标准局改名为新加坡生产力及标准委员会,简称SPRING。随着新加坡生产力及标准委员会2002 年法规及消费者保护 (安全规定) 2002年法规的实施,新加坡消费者保护(安全规定) 登录方案也同时己从官方验证改为第三者符合性评估验证单位 (Conformity Assessment Body, CAB) 验证。
PSB Mark

PSB Safety Mark

PSB Test mark
技术信息
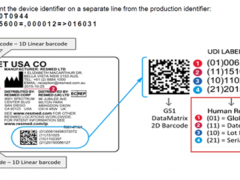
新加坡工商局公布消费品——公告的列管货物(ConTROLLED GOODS),必须符合安全标准要求。新加坡保护消费人士(安全规格)注册方案亦有此要求。
在列管电气产品需强制申请PSB认证,产品进入新加坡之前,必须由在新加坡有税籍之公司行号做为申请PSB之持证者(本公司提供新加坡商,可作为进行申请PSB认证时之持证者)。产品于取得PSB之后,方可进入新加坡销售。
发证 单位PSB (Productivity and Standard Board of Singapore)。a. 证书持有者为新加坡当地之公司行号,无工厂检查及年费。b. 证书有效期限:三年。c. 产品若有Plug,需提出SS246测试认证报告d. 产品认证无“系列”申请(每张证书只能涵盖单一型号
1. 新加坡电压为AC 230V/50Hz
2. 证书持有者需是当地注册之代表公司
发证 :安全标志需置于产品上
文件要求: 安全性测试
- 有效期在三年内的CB证书和测试报告(仅英文版)
- 由PSB Corporation 或认可测试实验室根据新加坡标准发出的所有报告
- 由新加坡实验室立案体系承认的独立实验室发出之报告
2. 附加文件
- 新加坡当地代表资料
- 新加坡安规申请授权信(新加坡当地代表公司信纸)
- 若CB证书持有人与新加坡当地代表公司不同, CB证书持有人须出示授权信
- 完整的电路/线路图(含额定值) ,以及零件表 (最好是A3尺寸)
- 英文使用手册
- 原版卷标或清楚可见的彩色照
- 彩色外观和内部照片
有需要申请认证或咨询问题的企业,请联系我们
苏州莱瑞测信息科技有限公司
莱瑞测 - 您身边的产品认证服务专家
电话:0512-68157565
邮箱:service@lairuice.com
手机:17314226061
微信:17314226061
印度尼西亚医疗器械注册要点
印度尼西亚作为东南亚最大的经济体之一,其医疗器械市场近年来展现出强劲的增长势头。印尼的医疗器械市场规模在过去几年中持续扩大,年增长率保持在较高水平。这一增长主要得益于印尼经济的稳定发展、人口的持续增长
0评论2025-05-26196
阿联酋医疗器械注册认证指南
一、基本概况1.自然环境阿拉伯联合酋长国简称阿联酋,位于阿拉伯半岛东部,北濒波斯湾,海岸线长734公里。西和南与沙特阿拉伯交界,东和东北与阿曼毗连。属热带沙漠气候,全年分两季,5至10月为热季,最高气温可达50
0评论2025-05-26181
医疗器械软件注册申报常见问题
问:软件如何进行命名?答:建议在《医疗器械分类目录》《医疗器械通用名称命名规则》和《医用软件通用名称命名指导原则》的框架下,再综合考虑同类已上市产品的名称规范申报注册产品的通用名。问:软件的交付方式有
0评论2024-09-04281
欧盟医疗器械CE注册流程
一、欧盟医疗器械CE注册流程1.你首先需要的是得到一个合格的PRRC(负责法规遵从性的人)。通常由同一个人担任ISO 13485定义的管理者代表。但是,这可以分包给合格的顾问(如CMS)。2.接下来,您需要根据医疗器械法规
0评论2024-09-04190
欧盟发布IVDR延长过渡期的常见问答
2024年7月9日,IVDR过渡期修正案Regulation (EU)2024/1860正式发布。其中更新后第110条讲述了遗留器械的过渡期时限和可以享受过渡期的条件。针对这份延期修正案,欧盟委员会发布了一份《体外诊断医疗器械法规》(IVD
0评论2024-08-09229
欧盟电暖器CE-ErP能效法规更新
法规信息法规名称:(EU) 2024/1103 生效日期:1 July 2025 对象:出口欧盟的电暖器产品主要变化:法规更新取代原法规(EU) 2015/1188更新内容1.管控范围商用局部空间加热器的管控范围由原来的120 kW以下,扩大到300 k
0评论2024-06-18223
浅析欧盟通用充电器的修订指令及指令指导文件
近些年由于ICT 技术的创新和快速发展,市场上的电子设备出现了各种类型的充电接口和充电解决方案,然而由于充电接口规格的不统一、不兼容,一方面带来了大量的电子垃圾,造成了电子资源的浪费,另一方面也给消费者带
0评论2024-06-18138
广东药监局医疗器械常见问题答疑汇总
1、《企业落实医疗器械质量安全主体责任监督管理规定》包含哪些内容?答:《规定》共六章三十条,主要包括三方面内容:一是明确质量安全关键岗位要求。生产企业质量安全关键岗位人员包括企业法定代表人和主要负责人
0评论2024-03-05177