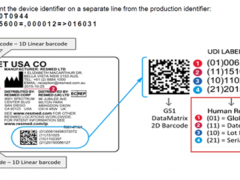
ENEC (European Norms Electrical Certification,欧洲标准电器认证) 是 CENELEC (欧洲执委会电工标准化组织)的一项认证计划,该计划是针对特定并符合欧洲标准的产品(如照明设备,组件,及办公室&数据设备)所使用的通用欧洲标准。
ENEC标志是欧洲安全认证通用标志,该标志是欧洲厂商基于调和欧洲安全标准进行测试的基础之上所采用的。
ENEC标志

在2000年3月于南斯拉夫召开的98CCA会议上,一致通过原来只允许欧洲制造商采用的“ENEC”标志开始对全世界所有制造商开放使用。
最初认证只针对IT(信息技术)设备(EN60950),但是现今“ENEC”标志的范围包括:
● 信息设备(EN60950)
● 变压器(EN60742,EN61558)
● 照明灯饰(EN60598)和相关文件(EN60920,EN60440)
● 电器开关(EN61058)
“欧洲标准电器认证”说明 – 出现在ENEC标志右边的数字是辨别CCA不同成员国的标识(译注:不同的数字代表不同的成员国/认证机构,例如17代表Nemko)。现在有21个成员国及23个认证机构。如果制造商希望的话,认证机构的标志也可以加上。ENEC是对消费者和有关当局证明该产品是经由高度公信力的第三方认证机构所认证。简而言之,该标志需要:
● 经过ENEC成员国认证机构的测试和认证。如:Nemko, Semko等
● 制造商的产品管理必须符合ISO9002,或于其相等的标准。
● 根据调和检查程序,最初的和最小年产量将受发证机构的检查。
● 每隔一年对认证过的产品进行有选择的重测。
认证机构与ENEC代码
| 代码 | 国家 | 认证机构 | 代码 | 国家 | 认证机构 |
| 01 | 西班牙 | AENOR | 13 | 瑞士 | SEV |
| 02 | 比利时 | CEBEC | 14 | 瑞典 | SEMKO |
| 03 | 意大利 | IMQ | 15 | 丹麦 | DEMKO |
| 04 | 葡萄牙 | CERTIF | 16 | 芬兰 | FIMKO |
| 05 | 荷兰 | KEMA | 17 | 挪威 | NEMKO |
| 06 | 爱尔兰 | NSAI | 18 | 匈牙利 | MEEI |
| 07 | 卢森堡 | SEE | 19 | 英国 | BEAB |
| 08 | 法国 | LCIE | 20 | 英国 | ASTA |
| 09 | 希腊 | ELOT | 21 | 捷克 | EZU |
10
| 德国 | VDE | 22 | 斯洛文尼亚 | SIQ
|
11
| 奥地利 | OVE | 24 | 德国 | TÜV Rheinland |
| 12 | 英国 | BSI |
|
|
|
印度尼西亚医疗器械注册要点
印度尼西亚作为东南亚最大的经济体之一,其医疗器械市场近年来展现出强劲的增长势头。印尼的医疗器械市场规模在过去几年中持续扩大,年增长率保持在较高水平。这一增长主要得益于印尼经济的稳定发展、人口的持续增长
0评论2025-05-26175
阿联酋医疗器械注册认证指南
一、基本概况1.自然环境阿拉伯联合酋长国简称阿联酋,位于阿拉伯半岛东部,北濒波斯湾,海岸线长734公里。西和南与沙特阿拉伯交界,东和东北与阿曼毗连。属热带沙漠气候,全年分两季,5至10月为热季,最高气温可达50
0评论2025-05-26161
医疗器械软件注册申报常见问题
问:软件如何进行命名?答:建议在《医疗器械分类目录》《医疗器械通用名称命名规则》和《医用软件通用名称命名指导原则》的框架下,再综合考虑同类已上市产品的名称规范申报注册产品的通用名。问:软件的交付方式有
0评论2024-09-04275
欧盟医疗器械CE注册流程
一、欧盟医疗器械CE注册流程1.你首先需要的是得到一个合格的PRRC(负责法规遵从性的人)。通常由同一个人担任ISO 13485定义的管理者代表。但是,这可以分包给合格的顾问(如CMS)。2.接下来,您需要根据医疗器械法规
0评论2024-09-04175
欧盟发布IVDR延长过渡期的常见问答
2024年7月9日,IVDR过渡期修正案Regulation (EU)2024/1860正式发布。其中更新后第110条讲述了遗留器械的过渡期时限和可以享受过渡期的条件。针对这份延期修正案,欧盟委员会发布了一份《体外诊断医疗器械法规》(IVD
0评论2024-08-09200
欧盟电暖器CE-ErP能效法规更新
法规信息法规名称:(EU) 2024/1103 生效日期:1 July 2025 对象:出口欧盟的电暖器产品主要变化:法规更新取代原法规(EU) 2015/1188更新内容1.管控范围商用局部空间加热器的管控范围由原来的120 kW以下,扩大到300 k
0评论2024-06-18210
浅析欧盟通用充电器的修订指令及指令指导文件
近些年由于ICT 技术的创新和快速发展,市场上的电子设备出现了各种类型的充电接口和充电解决方案,然而由于充电接口规格的不统一、不兼容,一方面带来了大量的电子垃圾,造成了电子资源的浪费,另一方面也给消费者带
0评论2024-06-18127
广东药监局医疗器械常见问题答疑汇总
1、《企业落实医疗器械质量安全主体责任监督管理规定》包含哪些内容?答:《规定》共六章三十条,主要包括三方面内容:一是明确质量安全关键岗位要求。生产企业质量安全关键岗位人员包括企业法定代表人和主要负责人
0评论2024-03-05168