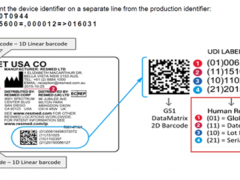
MET美国产品认证公司是美国著名的认证机构,1959年成立于美国马里兰州。MET因其在开发产品测试技术和认证标准的杰出表现而享有盛誉。将近半个世纪以来,MET在美国专注于高科技产品的认证和测试。时至今日,MET已经成为高科技产品认证的著名品牌。同时,带有MET认证标志的消费类电器广为北美著名零售商所接纳。
目前MET提供的服务项目包括产品安全认证、电磁兼容、可靠性测试、通信产品测试四大类,所涉及到的行业包括汽车、电缆、家电、光纤产品、医疗设备、通信设备、无线设备、NEBS、射频识别(RFID)、军工产品等。MET是美国极为少数能获得如此全面资质的测试及认证机构。其中一些资质更是属于世界上最难获得的资质,如全球唯一的射频识别(RFID)认证机构。
根据美国与欧洲相互认可协议,MET还可进行欧盟的R&TTE,EMC,LVD的检测,颁发欧洲合作NB的证书。MET是CB体系的认证机构(NCB)及测试机构(CBTL).至此,MET可以为客户提供全球“一站式”便利快捷的专业服务。
MET 认证标志

服务项目
MET的安全认证标志与UL标志在北美地区具备同等效力。MET可对多种电子、家用电器、电信设备,医疗设备、电动工具等电气产品进行美国政府和加拿大政府承认的检测和认证。
MET可以给客户提供广泛的测试和认证服务。目前我们的服务项目包括:产品安全认证,无线与电磁兼容,通信与NEBS, 国防军工产品,以及产品可靠性测试等。涉及的行业包括:汽车电子,特种线缆,消费类电器,通讯,医疗,军工产品等等。
申请须知
在询价阶段,客户应尽可能提供以下材料,以便迅速处理
1) 产品描述,如产品名称、型号、参数、用途以及所需服务
2)电气原理图,线路板的布线图
3)产品手册,手册应包括产品功能、操作指引等
4) 产品关键零件清单
5) 产品外观图、内部图,有图片更好
在申请阶段,客户应尽可能提供以下材料,以便项目顺利进行
1)签署认证申请表
2) 签署报价单
3)产品具体描述: 产品名称、型号、参数、铭牌、用途
4)具体的电气图、电路板的布线图
5)产品上附带的各种标志、标签、警告语
6)完整的产品手册,包括产品主要功能的描述、用户指引、重要提示等
7) 关键零件清单和零件的认证证书。如果产品上的零件中包括(但不仅限于)变压器、滤波组件、转换器、马达等,客户需要同时按MET的要求提供该零件的详细规格书
8)如果测试中需要额外的零件,客户应按MET的要求提供备用零件。一般指不浸漆的变压器、保险
丝、整桥二极管、电源FET等。
工厂检验
工厂检验是产品认证不可缺少的一环,也是工厂产生认证成本的最直接来源。因此,清楚工厂检验的要求、明确认证成本的根源是制造商进行认证管理的首要任务。
其次,在解决以上问题的基础上,制造商需要建立起一套具备操作性的认证管理体系对产品认证涉及的各个方面进行管理,持续改善去满足管理认证的要求。
再次,制造商将认证管理纳入到已有的管理体系中,并进行系统的优化,才可能产生协同效应。如果过分追求独立的认证管理体系,将不可避免的产生过多的管理费用。
此外,认证管理的操作中应该重视文化的影响因素。因为认证尤其是国外认证,往往涉及到跨文化的沟通问题,需要注意的文化心理的差异导致沟通行为的不同。